Propriedades das Substâncias Químicas – Parte 1
Tratar de riscos químicos é algo que gera medo em muitos prevencionistas.
Boa parte disso se deve ao desconhecimento da “linguagem” da química e das propriedades das substâncias.
Nesse artigo, vamos discutir as principais propriedades que estão associadas à exposição ou não do trabalhador a um dado agente.
Isso porque, em muitos casos, o agente está lá, mas não há de fato exposição a ele. E, se não há exposição, não há RISCO.
Vejamos um exemplo bem grosseiro: um pedaço de granito em uma bancada de cozinha tem sílica em sua composição. Mas, enquanto a bancada estiver lá “parada”, você não está exposto à sílica.
Isso ocorrerá apenas quando a pedra for cortada.
O mesmo, de forma menos evidente, acontece com muitos produtos químicos usados nas empresas.
Então, nesse contexto, vamos apresentar as seguintes propriedades:
- Volatilidade (ponto de ebulição e pressão de vapor);
- Densidade relativa de vapor.
Também falaremos sobre o ponto de fulgor (ou ponto de inflamação), que é uma propriedade cujo conhecimento é importante para o nosso cotidiano.
Essas propriedades costumam estar discriminadas na Seção 9 das FISPQ:
Vamos lá!
Volatilidade
A volatilidade é uma propriedade muito importante em substâncias líquidas: quanto mais volátil ela for, mais vapor do produto poderá existir no ambiente de trabalho. Em consequência, a exposição será maior.
A volatilidade pode ser avaliada através de duas propriedades que estão conectadas: temperatura de ebulição e pressão de vapor.
A temperatura de ebulição de uma substância (ou ponto de ebulição) é aquela em que ela passa do estado líquido para o gasoso.
Assim, quanto menor a temperatura de ebulição de uma substância, mais fácil ela evapora, e maior é a quantidade do seu vapor que poderá existir em um ambiente de trabalho.
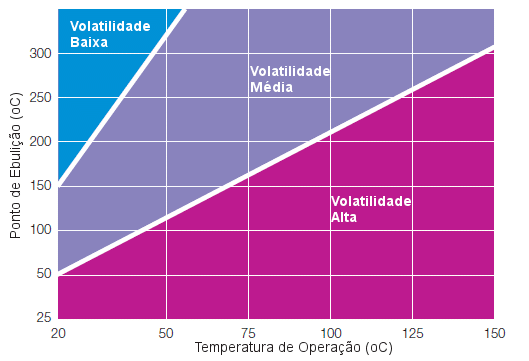
No nosso artigo sobre Avaliação Qualitativa/Control Banding, apresentamos a figura abaixo, que é usada para classificar a volatilidade de uma substância líquida:
Apresentamos também a tabela a seguir, que relaciona as bandas de volatilidade à pressão de vapor:

Perceba que há uma relação inversa entre essas propriedades:
- Temperatura de ebulição alta, pressão de vapor baixa: volatilidade baixa.
- Temperatura de ebulição baixa, pressão de vapor alta: volatilidade alta.
Para uma definição “amigável” sobre o que exatamente é a pressão de vapor, consulte aqui:
https://pt.wikipedia.org/wiki/Press%C3%A3o_de_vapor
Densidade Relativa de Vapor
Enquanto a volatilidade da substância se relaciona à sua capacidade de liberar vapor no ambiente, a densidade relativa de vapor se refere ao “peso” desse vapor: grosseiramente falando, ele tende a “subir” ou “descer”?
Ela é “relativa” porque está relacionada à densidade do ar atmosférico.
Então:
- Quanto menor a densidade de vapor de uma substância, mais ela também tende a se dispersar no ambiente de trabalho.
- No caso de densidades mais elevadas, isso indica que o vapor é “pesado” e tende a “descer”, ficando próximo ao chão ou à superfície de que foi liberado…
Isso é bem importante quando se pensa em sistemas de detecção: se uma substância tende a descer e os sensores são colocados acima do nível em que ela é liberada, ela não vai ser detectada, o que poderá provocar acidentes graves.
Essa propriedade também nos ajuda a entender alguns acidentes em espaços confinados, em que o gás sulfídrico fica no fundo dos tanques: sua densidade relativa de vapor é de 1,2.😉
Ponto de Fulgor (ou Ponto de Inflamação)
Apesar de não ser uma propriedade tão relacionada à exposição do ponto de vista da Higiene Ocupacional, entender o ponto de fulgor é importante para entender se uma substância é inflamável ou não.
Segundo o Manual para Interpretação de Informações sobre Substâncias Químicas da Fundacentro:
Ponto de fulgor é a temperatura acima da qual um líquido inflamável deve estar para que possa pegar fogo.
É importante registrar que, nessa temperatura, o fogo não se sustenta. A temperatura em que o fogo se mantém é o ponto de combustão.
Em ambos os casos, é necessária uma fonte de calor externa.
O importante para nós, por enquanto, é saber que quanto mais baixo o ponto de fulgor, mais inflamável é a substância.
Para fins de classificação na NR-20, amplamente negligenciada por aí, consulte esse artigo aqui:
https://www.sabersst.com.br/liquidos_inflamaveis_combustiveis/
E agora?
É MUITO importante estudar os processos produtivos (inclusive aspectos como pressões e temperaturas), saber as matérias-primas envolvidas e, a partir daí, pesquisar os possíveis subprodutos.
Com essas informações, podemos buscar as propriedades das substâncias envolvidas e então determinar melhor o cenário em que o trabalhador está e sua real exposição.
Um exemplo bem interessante está nas galvanoplastias.
Na etapa de decapagem em um banho de ácido sulfúrico ou ácido clorídrico, por exemplo, você poderia imaginar que não haveria exposição ao ácido por via respiratória; afinal, a temperatura de ebulição do ácido é maior que a do banho.
No entanto, o processo de decapagem forma gás hidrogênio. Esse gás “arrasta” o ácido, formando uma névoa (lembrando que névoa é particulado líquido)1. E névoas de ácidos fortes são classificadas como cancerígenas pelo IARC…
É difícil? Não, mas requer repertório. E isso só se adquire lendo, conversando com outros profissionais e vivendo a SST a cada dia, conscientes de que nunca saberemos tudo – e não tendo medo disso.
Façamos todos um bom trabalho!
Fontes:
- 1 Um estudo crítico sobre a saúde dos trabalhadores de galvânicas por meio das relações entre as avaliações ambientais, biológicas e otorrinolaringológicas. Carlos Sérgio da Silva. FUNDACENTRO, 2010.
- Manual para interpretação de informações sobre substâncias químicas. José Tarcísio Buschinelli e Mina Kato. FUNDACENTRO, 2012.


Boa noite Cibele,
Como sempre,excelente trabalho.
Parabéns!
Obrigada, Claudio! 🙂